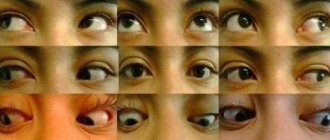
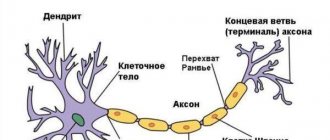
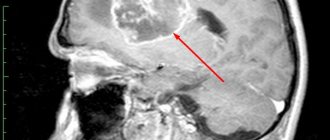
Группа нейродегенеративных заболеваний
Данная группа болезней характеризуется поражением центральной нервной системы. Определенное количество нейронов погибает, а это приводит к неврологическим патологиям. Нейродегенеративные заболевания могут иметь разные причины возникновения и разные клинические проявления. Характерно, что все болезни данной категории неизлечимы. Вся терапия, которая применяется, является симптоматической. То есть она облегчает проявление болезни, но никак не способствует регенерации поврежденных участков. Наиболее эффективной была бы трансплантация нервной ткани, однако метод имеет как технические, так и моральные препятствия. К подобным болезням можно отнести заболевание Альцгеймера, Паркинсона, Фара. Как правило, диагностика таких болезней на ранних стадиях утруднена. Чаще всего при постановке диагноза специалисты опираются на жалобы пациентов и результаты наблюдений за их поведением. Но главным инструментом является томография (компьютерная, магниторезонансная).
Общие сведения
Основными характеристиками группы дегенеративных заболеваний ЦНС являются следующие критерии:
- заболевания начинаются незаметно, до их появления нервная система могла работать абсолютно нормально;
- заболевания имеют постепенно прогрессирующее течение, могут длиться годы или десятилетия;
- некоторые дегенеративные заболевания связаны с наследственными факторами и развиваются у нескольких членов одной семьи;
- нейродегенеративное заболевание ЦНС характеризуется постепенной гибелью нейронов и заменой их глиальными элементами;
- атрофические процессы на начальной стадии развития патологии возникают в каком-либо определенном участке одного из полушарий головного мозга; далее в периоде развернутой стадии дегенерации атрофия в головном мозге становится практически симметричной.
Различные заболевания ЦНС, список которых достаточно длинный, остаются на стадии изучения. Достоверно неизвестны причины возникновения атрофических процессов при нормальном функционировании нервной системы большую часть жизни человека. Тем не менее, существует ряд факторов, которые могут провоцировать дегенерацию головного мозга:
- злоупотребление алкоголем, наркомания;
- токсическое влияние пестицидов и гербицидов;
- менингококковая инфекция;
- вирусные энцефалиты;
- дефицит витамина В12 и фолиевой кислоты.
Опасность дегенеративных заболеваний ЦНС состоит в том, что их сложно предвидеть. При наличии провоцирующих факторов в жизни человека рекомендуется вести здоровый образ жизни и регулярно посещать невролога для профилактических осмотров. Заподозрив признаки заболевания ЦНС, следует немедленно обратиться к врачу. Чем раньше будет выявлено заболевание, тем больше шансов замедлить прогрессирование дегенеративных процессов в головном мозге.
Диагностика и лечение дегенеративных заболеваний будет зависеть от вида патологии. Определив клиническую картину болезни, врач назначит исследования для уточнения состояния пациента. Они могут включать лабораторные анализы, УЗИ, МРТ, КТ, и психологические тесты для определения состояния когнитивных навыков.
В Юсуповской больнице города Москвы работает клиника неврологии, в которой оказывают помощь высококвалифицированные неврологи, доктора наук. Врачи Юсуповской больницы имеют большой опыт лечения дегенеративных заболеваний ЦНС и используют в своей работе новейшие методики терапии и реабилитации, что позволяет браться за самые сложные случаи.
Обратиться за помощью, записаться на прием и получить консультацию специалистов можно по телефону.
Врач-невролог, руководитель клиники хронической боли
Список таких заболеваний довольно велик, а встречаются они настолько часто, что врачи уже сегодня говорят о нейродегенерации как о большой проблеме XXI века. В лидерах «убийц нейронов» — Альцгеймер и Паркинсон, вернее, заболевания, названные в честь описавших их ученых.
Принято считать, что эти патологии, как и в целом нейродегенеративные заболевания — удел пожилых людей. Однако есть немало случаев, когда обе болезни начинаются в молодом возрасте, буквально сразу, как только головной мозг перестает расти.
И именно в молодости, в основном, развивается гиперпролактинемия, патология, при которой вырабатывается слишком много гормона пролактина. Гибель нейронов при этом заболевании вызывает торможение репродуктивной функции, бесплодие, а на запущенной стадии болезнь провоцирует гипофизарную опухоль.
Выделяют две группы нейродегенеративных заболеваний: спорадическую и ирритативную. К спорадическим относят болезнь Альцгеймера, мультисистемную атрофию, паркинсоническую деменцию, прогрессирующий надъядерный паралич, деменцию с тельцами Леви.
К ирритативным — болезни Вильсона-Коновалова, Галлервордена-Шпатца, Фара, Бессена-Корнцвейга и хорею Геттингтона.
Болезнь Фара включает случаи первичного идиопатического отложения кальция в мозговых структурах, вторичные формы церебрального кальциноза в рамках данной патологии не рассматриваются. Первые подробные описания заболевания сделаны в 1930 году немецким невропатологом К.Т. Фаром. Болезнь Фара является редкой нозологией, распространённость составляет менее 1 случая на 1 млн. населения.
ПОДРОБНЕЕ: Мозжечковый синдром, как симптом и следствие неврологических нарушений
Гендерные различия в заболеваемости выражаются соотношением мужчин и женщин 2:1. Патология проявляется в любом возрастном периоде, чаще в 30-60 лет. Прижизненно выявляется лишь в 1-2% случаев, что объясняется наличием бессимптомных вариантов течения, диагностикой заболевания под видом иных нейродегенеративных процессов (болезни Паркинсона, сенильной хореи).
Болезнь Фара
Симптоматика заболевания
Так как данная болезнь – явление довольно редкое, то специалистам сложно предоставить правильную клиническую картину синдрома. Симптомы могут проявляться, если возраст пациента превышает 40 лет. У более молодых людей болезнь Фара симптомы может иметь смазанные и нечеткие. У пациентов нарушается координация движения, паркинсонизм. Также о развитии заболевания могут свидетельствовать такие признаки, как тремор, дистония, быстрые и беспорядочные движения конечностей (хорея), непроизвольные сокращения кистей, стоп. Так как болезнь поражает участки головного мозга, то снижается работоспособность, умственные возможности. Страдает также и память человека. Часто нарушается и речь. К другим неврологическим признакам можно отнести болевые ощущения, расстройства психики. Различают ювенильную форму заболевания, которая проявляется у детей, подростков. Основные симптомы при этом таковы: дистония, хорея, припадки эпилепсии. Сенильная форма характерна для лиц среднего и более пожилого возраста. В этом случае наблюдается паркинсонизм, нарушения речи, другие проблемы в работе нервной системы. Также может возникнуть недержание мочи.
Классификация
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
- Ювенильная форма — дебют заболевания происходит в детском или подростковом периоде. Характерны экстрапирамидные нарушения в виде атетоза, хореи, мышечной дистонии. Патология может сопровождаться олигофренией. По мере взросления отмечается смена гиперкинезов паркинсонической симптоматикой.
- Сенильная форма — манифестирует в пожилом и среднем возрасте. Клиническая картина характеризуется доминированием симптомов паркинсонизма в сочетании с когнитивными расстройствами. Типична прогрессирующая деменция.
В практической неврологии болезнь Фара подразделяется на две клинические формы, отличающиеся возрастом манифестации, типом преобладающей симптоматики:
- Ювенильная форма — дебют заболевания происходит в детском или подростковом периоде. Характерны экстрапирамидные нарушения в виде атетоза, хореи, мышечной дистонии. Патология может сопровождаться олигофренией. По мере взросления отмечается смена гиперкинезов паркинсонической симптоматикой.
- Сенильная форма — манифестирует в пожилом и среднем возрасте. Клиническая картина характеризуется доминированием симптомов паркинсонизма в сочетании с когнитивными расстройствами. Типична прогрессирующая деменция.
Возможные причины возникновения синдрома Фара
Причины, из-за которых возможно развитие болезни, точно не установлены. Однако известно, что огромное влияние на ее возникновение имеют нарушения работы щитовидной, паращитовидной желез. При этом происходят сбои в обменных процессах кальция, фосфора. Подобные нейродегенеративные заболевания могут возникнуть и при нарушениях кислотно-щелочного баланса в организме. Алкалоз приводит к значительной потере кислот. А вот щелочные соединения присутствуют в избытке. Существует также мнение, что синдром Фара проявляется при генетических нарушениях. То есть мутирует ген, который отвечает за обмен такого элемента, как кальций. Однако у такой версии есть много противоречий. Известны единичные случаи, когда симптомы заболевания проявлялись после облучения области головы, отравления ядами, свинцом, у детей с синдромом Дауна. Также кальциноз был диагностирован у людей, переболевших краснухой (редко). Еще одна возможная причина кальцификации базальных ганглиев – родовые травмы.
Методы исследования для постановки диагноза
До возникновения компьютерной томографии больным проводились рентгенологические исследования головного мозга. Благодаря появлению современных методов исследования, специалисты получили более информативные картинки с пораженной зоны. Однако стоит отметить, что большей чувствительностью при данной клинической картине обладает компьютерная, а не магнитно-резонансная томография. При анализе большинства снимков пораженные участки ограничиваются бледным шаром. Имеют они небольшие размеры. Чаще всего терпят изменения базальные ганглии, таламус, мозжечок. Уровень кальцинации примерно одинаковый что у молодых, что у пожилых людей. Также не обнаружены различия между группами, у которых болезнь Фара протекает бессимптомно, и тех, где синдром сопровождается ярко выраженными признаками.
Гистологические исследования
При проведении патологоанатомического исследования в головном мозге наблюдают следующую картину: сосуды имеют белесоватый вид (некоторые ветвистые участки). При прикасании ножа они издают звук, похожий на хруст. Для гистологического анализа проводится забор материала: срезы коры головного мозга, базальных ганглиев, мозжечка. Именно в области последних кальцификация встречается чаще всего. На образцах присутствуют соли кальция. Также чаще всего они выявляются на артериях (мелких, средних), капиллярах. Реже (единичные случаи) болезнь Фара поражает вены. По всей длине сосудов, а также в прилегающих тканях обнаруживаются конгломераты кальция маленьких размеров. Также в тканях выделяют присутствие следов мышьяка, алюминия, кобальта, мукополисахаридов.
Патогенез
Формирующие болезнь патогенетические механизмы окончательно не определены. Предполагаются генетически детерминированные сдвиги церебрального метаболизма, становящиеся причиной отложения в мозговых тканях избытков кальция. Выраженная кальцификация подкорковых образований становится причиной дезорганизации лобно-субкортикальной системы, регулирующей произвольные движения и обеспечивающей когнитивные функции (память, мышление, внимание).
Морфологически кальцификаты обнаруживаются симметрично в различных структурах: коре мозга, белом веществе, подкорковых ганглиях, внутренней капсуле, мозжечке, стенках мелких артерий, реже вен. Характерно наличие периваскулярных мелких кальциевых конгломератов. Наиболее массивная кальцификация выявляется в подкорковых отделах.
Постановка диагноза
В зависимости от того, имеет ли болезнь Фара симптомы, постановка диагноза может несколько утрудняться. Нередко ее диагностируют случайно, проводя томографию для подтверждения совсем другого заболевания. Прежде всего, специалист исключает нарушение обмена кальция, других пороков развития. Затем назначается компьютерная томография (или же рентгенологические исследования). Врачи отмечают, что одной из проблем в постановке правильного диагноза является гипопаратиреоз. Это заболевание, которое возникает при дефиците паратгормона. Вследствие этого уровень кальция в крови снижается, а уровень фосфора растет. Если при компьютерной томографии наблюдается кальцинация стриопаллидозубчатых структур, то того, чтобы отличить гипопаратиреоз от такого состояния, как болезнь Фара, необходимы дополнительные анализы. Прежде всего, важно определить уровень паратгормона и кальция. Также при постановке диагноза используется паразитарное поражение нервной системы. Возникают специфические реакции в крови, спинномозговой жидкости. Нечасто болезнь Фара дифференцируется с таким состоянием, как склероз Бурневилля.
Нейродегенеративные болезни: не только у пожилых
Все эти заболевания, имеющие нейродегенеративные нарушения, лечению не поддаются. Эти процессы, происходящие в коре головного мозга и ЦНС, необратимы и погибшие нервные клетки не могут восстановиться и возобновить утраченные функции.
На пациенте не ставится крест, он наблюдается у врача с регулярностью, которую устанавливает ведущий специалист. Лечащий врач разрабатывает комплекс медикаментов, которые служат поддержкой и отсрочкой больного. Они направлены на замедление прогресса болезни, устранение некоторых симптомов и снятия болевых синдромов.
Такие пациенты требуют постоянной заботы и ухода за ними, ведь выполнять множество вещей самостоятельно они уже не в силах. Их нельзя оставлять без присмотра, но и в обществе их нахождение небезопасно, поэтому стоит их изолировать. Комплексное лечение включает в себя поддержку родных и близких, которая незаменима в процессе лечебных мер.
Перечень медикаментов выписывается сугубо индивидуально, потому как каждый отдельный случай уникален в своем роде. Направление лечения зависит от причин, спровоцировавших недуг, осложнений и особенностей организма больного. Для улучшения питания мозга назначаются ноотропы, для успокоения нервной системы нейролептики, успокоительные, в некоторых случаях антидепрессанты.
Эти сложные заболевания нередко вызывают глубокие депрессивные состояния пациентов, которые могут иметь склонности к суициду, поэтому нуждаются в сильнодействующих препаратах, но все они имеют множество побочных эффектов. Они могут корректировать и меняться за период лечения, подбираться другая доза.
Для каждого пациента разрабатывается комплекс тренировочных упражнений, которые улучшают состояние памяти и интеллекта, но свою пользу они будут иметь лишь на начальных стадиях, когда прогресс болезни не такой сильный и пациент не утратил ум полностью.
Важно следить за питанием, рационом и регулярностью, ведь из-за плохой памяти и забывчивости пациент может пропускать основные приемы пищи. Лучше кормить больного строго по времени, используя специальную диету.
Народные средства в этом случае абсолютно бессильны, не существует замены сильным медикаментозным средствам. Можно использовать настои и отвары лишь как дополнительное средство, также допускается прием спиртовых настоек.
Поскольку патогенез заболевания остаётся неясным, терапия имеет преимущественно симптоматический характер. С целью улучшения обменных процессов применяются стимуляторы тканевого метаболизма (ацетилкарнитин, глютаминовая кислота, комплекс L-цитруллин малат, никотинамид), цитопротекторы (рибофлавин, янтарная кислота, мельдоний).
При симптомах паркинсонизма предпочтительно назначение фармпрепаратов леводопы, при гиперкинезах — холинолитиков, бензодиазепинов. Наличие эпилептических приступов служит показанием к лечению современными антиконвульсантами (леветирацетамом). В комплексной терапии применяется лечебная физкультура, водолечение, когнитивные тренинги.
В настоящее время нет эффективного лечения, устраняющего причину заболевания. В зависимости от симптомов применяются различные лекарства для снятия или подавления симптомов болезни Фара. В случае появления признаков депрессии, тревоги или других психических расстройств применяется медикаментозное лечение, применяемые стандартно против этим заболеваниям.
ПОДРОБНЕЕ: Лечение синдрома раздраженного кишечника
Эпилепсия лечится противоэпилептическими препаратами, оксибутинин нашел применение при недержании мочи. На ослабление двигательных расстройств иногда благоприятно влияет на регулирование кальций-фосфат-дегидрогеназы. Из-за различий в выраженности симптомов, трудно, однако, предсказать прогноз у конкретного человека, у которого появилась болезнь Fahra. Смертность в случае возникновения этого заболевания велико. Заболевание может привести также к прогрессирующей инвалидности.
Лечить нейродегенеративные заболевания мы пока не умеем, хотя и знаем о них очень давно. Можно только проводить симптоматическую терапию, замедлять некоторые болезни, облегчать состояние.
Но сегодня уже есть прорывы в диагностике: ученые говорят о том, что первые признаки болезней Альцгеймера и Паркинсона можно определять в самом начале, когда гибель нейронов еще никак не отражается на человеке внешне, и он чувствует себя вполне здоровым.
Такая диагностика пока не массовая. Но вот, что точно можно сделать уже сегодня — это начать профилактику таких болезней. Она несложная. Все, что требуется — это здоровый образ жизни с физическими нагрузками, изменение питания (отлично работает средиземноморская диета) и активные нагрузки на мозг: шахматы, садоводство, изучение иностранного языка или игра на музыкальных инструментах.
Все это — залог образования новых связей между такими маленькими, но важными для нас нейронами.
Старческое слабоумие: можно ли избежать?
Здоровье
Лечение
Удаление скоплений кальция, которые образовались в головном мозге и его сосудах, является невозможным. Как правило, лечение подобного заболевания носит симптоматический характер. Прежде всего, оно направлено на улучшение обмена кальция и фосфора в организме. Если наблюдаются симптомы болезни Паркинсона, то специалист назначает специальные препараты (леводопы). Также болезнь Фара, лечение ее проявлений, предполагает прием антиоксидантов, средств для улучшения метаболизма. Терапия блокаторами кальциевых каналов неэффективна. Стоит учесть тот факт, что заболевание довольно редкое и малоизученное. В большинстве случаев терапия ослабляет симптомы проявления болезни, однако на степень кальцификации не влияет.
Глава 2.: «Болезнь Фара»
Книга: «Редкие неврологические синдромы и болезни» (В.В. Пономарев)
Болезнь Фара (идиопатическая неатеросклеротическая симметричная интрацеребральная кальцификация базальных ганглиев) — редкое нейродегенеративное заболевание, впервые описанное Т. Fahr в 1930 г. [3]. Характерным рентгенологическим признаком болезни Фара (БФ) является массивная кальцификация подкорковых ганглиев (чаще бледного шара) и колена внутренней капсулы. Реже аналогичные нарушения носят распространенный характер и обнаруживаются в полушариях мозга и мозжечке [5, 6, 12]. Клинические проявления БФ разнообразны и не коррелируют с морфологическими данными. Неврологические симптомы заболевания включают различные экстрапирамидные нарушения (ригидность, тремор, гиперкинезы), преходящие или стойкие пирамидные знаки, эпилептические приступы, деменцию [1, 2, 7]. В клинической картине БФ нередко отмечаются проявления гипер- или гипопаратиреоза в форме фокальных судорог, тетанических спазмов, болей в дистальных отделах конечностей, положительные симптомы Хвостека и Труссо [8, 11].
БФ встречается в любом возрасте. Условно выделяют три группы больных:
1) молодые люди с признаками церебрального кальциноза; 2) пациенты с гипопаратиреозом; 3) пожилые больные с относительно небольшой кальцификацией [5].
Этиология БФ окончательно не установлена. Главным патогенетическим механизмом развития заболевания является нарушение фосфор-кальциевого метаболизма. Его основной причиной считается первичный (аутоиммунный) или послеоперационный эндокринный аденоматоз щитовидной либо паращитовидной железы [7, 9, 12]. Другим возможным механизмом развития заболевания называют хронический респираторный алкалоз, приводящий к различным электролитным нарушениям (гиперкальциемии, гипонатриемии) и, как следствие, к развитию гипоксии мозга [1, 8, 11]. Существует мнение о генетических механизмах нарушения обмена кальция при БФ, идентифицированных с определенным локусом 14q хромосомы [4]. Терапия заболевания носит симптоматический характер либо направлена на улучшение кальций-фосфорного обмена.
За 15 лет из 45 тыс. выполненных КТ-исследований головного мозга в 22 случаях (0,04%) мы наблюдали массивную кальцификацию головного мозга, и только у 2 больных имела место клиническая симптоматика. Приводим эти наблюдения.
Больной 3., 39 лет, сварщик, при поступлении в неврологическое отделение 5-й клинической больницы г. Минска жаловался на общую скованность и замедленность движений. Болен 4 месяца, когда без видимой причины заметил замедление движений в левой руке, затем общую скованность, изменилась походка. Амбулаторно получал недифференцированное лечение. Госпитализирован в связи с прогрессирующим ухудшением состояния.
Из ранее перенесенных заболеваний отмечает редкие простудные и легкую черепно-мозговую травму (15 лет назад). Аналогичные заболевания в семье отрицает. При поступлении состояние удовлетворительное, пониженного питания, АД 120/80 мм рт. ст. Щитовидная железа не увеличена, соматической патологии не выявлено. Сознание ясное, снижена память и критика к своему состоянию. Речь монотонная, лишена модуляций. Нарушена поза (поза просителя), лицо гипомимично, руки приведены к туловищу (рис. 17). Выражены рефлексы орального авто-матизма. Сила в конечностях достаточная, мышечный тонус повышен по пластическому типу. Отмечаются умеренные олиго- и брадикинезия. Сухожильно-периостальные рефлексы высокие, вызываются с расширенных зон D=S, подошвенные и брюшные рефлексы средней живости, патологических стопных знаков нет. Координация и чувствительность не расстроены. Походка изменена по типу микробазии, отсутствуют содружественные движения рук.
При обследовании: общеклинические анализы крови и мочи без патологии. Электролиты крови: калий 4,4 ммоль/л (норма 3,6-5,4 ммоль/л), натрий 136 ммоль/л (норма 130-150 ммоль/л), кальций 2,0 ммоль/л (норма 2,0-2,75 ммоль/л), фосфор 1,0 ммоль/л (норма 0,8-1,48 ммоль/л). Окулист: острота зрения OD/OS = 0,9/0,7, не корригирует, глазное дно без патологии. КТ головного мозга: субкортикально в лобных, височных, затылочных долях больших полушарий, базальных ганглиях, полушариях мозжечка определяются массивные симметричные участки обызвествления. Базальные цистерны, желудочки мозга, кортикальные борозды расширены (рис. 18). Радиоизотопное исследование щитовидной железы: железа шаровидной формы, распределение изотопа равномерное.
Рис. 17. Больной 3., 39 лет, с диагнозом болезнь Фара: поза «просителя», руки приведены к туловищу, лицо гипомимично
Рис. 18. КТ головного мозга этого же больного: субкортикально в лобных, височных, затылочных долях больших полушарий, базальных ганглиях, полушариях мозжечка определяются массивные симметричные участки обызвествления
Проведено лечение: мадопар (625 мг/сут), пирацетам, витамин Е, курс гипербарической оксигенации. На этом фоне состояние больного улучшилось, уменьшилась выраженность акинетико-ригидного синдрома. При катамнестическом наблюдении в течение трех лет признаков прогрессирования заболевания не отмечено. Обследованы дети больного: дочь (15 лет), в раннем детстве наблюдалось несколько эпилептических припадков, в течение года принимала противосудорожные средства. В настоящее время жалоб нет, при осмотре неврологической симптоматики не выявлено, КТ головного мозга без патологии. Сын (12 лет) жалоб не предъявляет, при объективном и КТ-исследованиях отклонений не обнаружено.
Второй больной Г., 21 года, слесарь, поступил с жалобами на повторяющиеся тонические судороги правой половины лица и конечностей продолжительностью 10—15 с, провоцируемые переменой положения тела, минимальной физической нагрузкой или внезапным обращением к нему. Болен 5 месяцев, когда после названных провоцирующих факторов изредка стали появляться вышеописанные пароксизмы. В последующем их частота увеличилась до 5—6 раз в сутки. С детства наблюдается в поликлинике по поводу врожденного аортального порока сердца и логоневроза. В 16 лет оперирован в связи с врожденным сходящимся косоглазием. Наследственность по данному заболеванию не отягощена. При поступлении состояние удовлетворительное, элементы дизрафического статуса (башенный череп, сросшиеся мочки ушей). АД 120/80 мм рт. ст., пульс 64 уд/мин, ритмичный. Щитовидная железа не увеличена. Аускультативно выслушивается систолический шум на верхушке и в точке Боткина. Другой соматической патологии не выявлено. Неврологически: в сознании, адекватен, память не нарушена, речь с элементами логоневроза. Черепные нервы без патологии. Сила и тонус в конечностях не изменены, сухожильно-периостальные рефлексы средней живости, D=S. Координация и чувствительность не нарушены. В отделении в течение первых 5 дней повторялись кратковременные (до 10 с) вычурные насильственные движения в правых конечностях без потери сознания, провоцируемые внезапными звуками или физической нагрузкой.
Определялись положительные симптомы Хвостека (судорожное сокращение мимических мышц при перкуссии в области ствола лицевого нерва) и Труссо (судорожное сокращение мышц кисти в виде «руки акушера» при сдавливании сосудисто-нервного пучка на уровне плеча).
Обследование: анализы крови и мочи без патологии. Электролиты крови: калий 3,9 ммоль/л, натрий 138 ммоль/л, кальций 1,9 ммоль/л, фосфор 2,0 ммоль/л. Окулист: острота зрения OD/OS = 0,9/0,2, не корригирует, глазное дно без патологии. ЭЭГ: регистрируются умеренные изменения биоэлектрической активности мозга на сниженном амплитудном уровне, признаков эпилептической активности не выявлено. КТ головного мозга: в полушариях мозга, базальных ганглиях, мозжечке определяются множественные симметричные очаги обызвествления. УЗИ щитовидной железы: изменений не выявило. Приступы мышечных спазмов купированы назначением малой дозы карбамазепина (100 мг/сут) и в последующем не повторялись.
Таким образом, в обоих представленных случаях рентгенологически обнаружены характерные признаки БФ. Клинические проявления заболевания существенно различались. У первого больного наблюдались явления паркинсонизма и деменции. У второго — преобладали клинические проявления первичного гипопаратиреоза на фоне перинатальной патологии ЦНС. У обоих больных положительные результаты были получены при назначении симптоматического лечения (леводопосодержащих и противосудорожных средств).
Классической триадой при БФ являются типичные нейропсихиатрические симптомы, гипопаратиреоз и симметричная кальцификация базальных ганглиев, однако данные литературы указывают, что чаще встречаются неполные формы заболевания [10]. С внедрением в повседневную клиническую практику современных методов нейровизуализации (особенно КТ головного мозга) прижизненная диагностика БФ облегчилась, так как эти исследования позволяют обнаружить признаки заболевания еще в доклинической стадии болезни. Несмотря на использование современных диагностических технологий, БФ встречается крайне редко. По данным различных авторов, рентгенологические признаки БФ отмечаются в 1—2% всех случаев проведения КТ головного мозга [5, 10]. При БФ кальцификация встречается во всех участках мозга, но преобладает в области базальных ганглиев [5, 6, 12]. Скопления кальция обнаруживаются вне кровеносных сосудов мозга и имеют характерную ультраструктуру. По данным A. Guseo и соавт. [6], кальцинаты состоят из тонких нитей (140-400 мк).
Клинические проявления БФ встречаются еще реже, чем рентгенологические. Так, Н. Goldscheider и соавт. [5] при проведении КТ головного мозга у 8000 больных в 19 случаях обнаружили кальцификацию базальных ганглиев, но только у 6 человек имелись клинические симптомы болезни. По мнению большинства авторов, неврологические расстройства не зависят от локализации и размеров очагов [5, 9]. К наиболее частым неврологическим проявлениям БФ относятся паркинсонизм и постепенно развивающаяся деменция, что ряд исследователей объясняют экстенсивным типом кальциноза и нарушением метаболизма нервной ткани [2, 12].
Нередко в клинической картине БФ встречается первичное (чаще аутоиммунное) или послеоперационное нарушение функции паращитовидной железы. В этих случаях изменение выработки паратгормона приводит к снижению содержания кальция и повышению фосфора в крови [7, 10]. При БФ описаны случаи псевдогипопаратиреоза при легочной патологии, когда вследствие гипервентиляции и гипокапнии увеличивается внутриклеточное содержание фосфора [8, 11]. Аналогичные механизмы развития гипоксии мозга объясняют кальцификацию мозга при гипертонической болезни [1]. D. Geschwind и соавт. описан семейный случай диагностики БФ с явлением генетической антиципации, при котором авторам впервые удалось идентифицировать хромосомный локус заболевания, картированный на 14q хромосоме [4].
Дифференциальный диагноз БФ проводят с паразитарным поражением нервной системы (токсоплазмоз, эхинококкоз, цистицеркоз). В этих случаях диагностическую ценность представляют эпидемиологический анамнез и специфические серологические реакции в крови и ликворе. Реже БФ дифференцируют с туберозным склерозом Бурневиля, при котором встречаются характерные изменения кожи.
В лечении БФ применяются симптоматические средства. При наличии симптомов паркинсонизма предпочтительнее использовать препараты леводопы (мадопар, синемет, наком), а не дофаминовые агонисты, так как в этих случаях большое значение приобретает заместительная терапия для восполнения дофамина. В качестве патогенетического лечения БФ показано назначение антиоксидантов, мозговых метаболитов, воздействие на электролитный состав крови.
Прогнозы при заболевании Фара
Так как данное состояние нарушает обмен веществ в головном мозге, а также соли кальция оказывают раздражающий эффект на его ткани, то болезнь Фара прогнозы имеет весьма неоднозначные. Заболевание прогрессирует медленно, с возрастом отложения кальция увеличиваются. Конечно, все это происходит не за один год. Как правило, нейродегенеративные заболевания прогрессируют в течение нескольких десятилетий. Основной проблемой является недостаток информации по данному состоянию, а также отсутствие специфического лечения. Поэтому терапия направлена на улучшение качества жизни пациента. Еще один негативный момент – болезнь плохо диагностируется на ранних стадиях.
Диагностика
Основным диагностическим методом, позволяющим неврологу достоверно установить наличие очагов кальциноза в мозговых тканях, является КТ головного мозга. Интенсивность очагов на томограммах отражает уровень концентрации кальция. МРТ головного мозга значительно хуже визуализирует кальцификаты, но позволяет оценить сопутствующие дегенеративные процессы. С целью подтверждения идиопатического характера патологии проводится целый ряд дополнительных обследований:
- Биохимический анализ крови
. Производится определение электролитов крови: кальция, фосфора, железа, натрия. Отсутствие существенных отклонений позволяет исключить общие обменные нарушения в организме, приводящие к отложению кальция. - Определение уровня паратгормона
. Нормальные показатели концентрации гормона в крови исключают наличие гипопаратиреоза, псевдогипопаратиреоза, как наиболее распространённых причин кальцификации. - УЗИ щитовиднойи паращитовидных желёз
. У пациентов с болезнью Фара эхоскопическая картина остается в пределах нормы, что исключает связанные с поражением этих желёз гормонально-обменные нарушения. - ТКДГ церебральных сосудов
. Необходима для оценки мозговой гемодинамики, выявления хронической церебральной ишемии как первопричины дегенеративных изменений, сопровождающихся кальцификацией. - ПЦР-исследования
. Направлены на выявление токсоплазмы, цитомегаловируса и других инфекционных агентов, способных вызывать воспалительные изменения мозговых тканей с образованием кальцификатов.
Диагноз болезнь Фара правомочен после исключения вторичного характера церебральной кальцификации, наблюдающейся при эндокринных (гипопаратиреоз, псевдогипопаратиреоз, гипотиреоз), сосудистых (атеросклероз, амилоидоз сосудов), инфекционных (краснуха, цистицеркоз, токсоплазмоз, цитомегалия) заболеваниях. Дифференциальная диагностика проводится также с болезнью Галлервордена-Шпатца, туберозным склерозом.